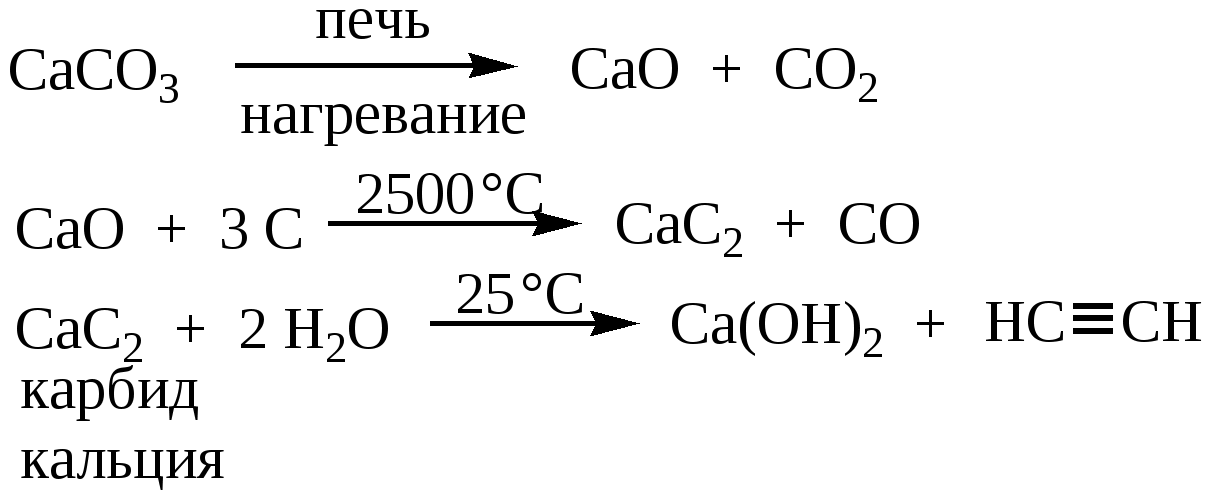Достоинства и недостатки
Достоинства у ацетиленовой сварки весомые. Во-первых, вам не нужно использовать электричество, чтобы произвести сварку. К тому же, все оборудование можно перевозить на специальной тележке, и вы сможете варить на улице в труднодоступных местах. Во-вторых, вы можете просто поменять угол направления пламени, и температура ванны сразу же изменится. Так можно довольно удобно регулировать степень нагрева.

В-третьих, при должной сноровке вы можете избежать прожогов просто меняя расстояние от сварочной ванны до горелки. Но не стоит забывать и о недостатках. Нужно понимать, что такая сварка требует много времени и терпения, поэтому ее нельзя назвать производительной.
А такой вариант вряд ли подойдет для крупного предприятия с большим количеством выпускаемой продукции. Также учитывайте, что во время сварки нагревается не только сварочная ванна, но и вся прилегающая область металла, а это не очень хорошо для детали. Также такую работу не сможет выполнить сварщик низкой квалификации, обязательно нужен профессионал своего дела.
Меры безопасности и хранение
Calcium carbide относится к 1 классу опасности по степени воздействия на организм. Его пыль раздражающе действует на кожные покровы, слизистые оболочки и дыхательные пути. Реагент очень опасен при вдыхании (симптомы: прерывистое дыхание, кашель, насморк, чувство удушья, отек легких), попадании на кожные покровы (получение ожогов, язв) и в глаза (резь, слезотечение, отек век).
При применении материала необходимо использовать специальную защитную одежду, противогаз, перчатки и специальную обувь. Работать только в хорошо проветриваемых помещениях. В случае попадания на кожу промыть пораженное место большим количеством воды, смазать жирным кремом и вызвать врача.
Хранить в герметичных тарах в вертикальном положении (не более, чем в 3 ряда) в несгораемых, хорошо вентилируемых складах или на открытых площадках под навесом, защищающих от воздействия влаги. Не допускается совместное хранение с другими веществами. Срок годности – 6 месяцев с даты производства.
Внешний вид и характеристики технического карбида кальция
Впервые рассматриваемый состав был получен в 1862 году. Проводимая процедура касалась отделения кальция от извести, в результате чего получился бледно-серый состав без признаков, свойственных металлам. В результате опыта был получен карбид, который в последствии стал активно использоваться при выпуске различной продукции.
В начале 20 века карбид кальция стали использовать для производства ацетилена в больших объемах. Именно поэтому стали вести активные исследования для выявления более производительной технологии.
Технические характеристики материала определяют его широкое распространение. Внешний вид вещества характеризуется светло-серым цветом, выпускаются карбиды в виде камня или порошка.
Методы получения карбидов
Карбиды могут быть получены взаимодействием углерода и его соединений с металлами или их соединениями. Известны следующие способы получения карбидов: 1) получение карбидов в литом виде;
2) науглероживание порошков металлов (или окислов) твердым углеродом;
3) науглероживание порошков металлов (или окислов) газами, содержащими углерод (часто в присутствии твердого углерода);
4) осаждение из газовой фазы (метод наращивания);
5) химическое выделение карбидной фазы или углеродистых ферросплавов или расплавов (метод растворения);
6) электролиз расплавов соответствующих солей.
Промышленное применение имеют первые три способа.
Получение литых карбидов основано на сплавлении металлов с углеродом и возможно только в электрической или высокочастотной печи, так как температуры образования и плавления карбидов тугоплавких металлов лежат в пределах 2500—4000° С. Это вызывает определенные технические трудности, поэтому способ получения литых карбидов имеет ограниченное применение.
Получение карбидов науглероживанием порошков металлов или окислов металлов твердым углеродом имеет наибольшее распространение и используется для промышленного приготовления карбидов вольфрама, титана, молибдена, тантала, ванадия и других карбидов, применяемых в производстве твердых сплавов.
В качестве исходного сырья при этом способе используют порошки чистых металлов или их окислов. Углерод вводят в смесь в виде тонкого порошка сахарного угля или сажи. Смесь металла (или окисла) с углеродом тщательно перемешивают в шаровых мельницах всухую или мокрым способом. При смешивании металла с твердым углеродом дают от 5 до 10% избытка углерода (по сравнению с теоретическим содержанием его), так как в металлических порошках имеется остаточный кислород, а также для компенсации частичного выгорания углерода в печи.
При использовании смесей окислов металла с углеродом учитывают науглероживающее действие образующейся окиси углерода и применяемого защитного газа. Обычно для реакции достаточно 80—90%-ного количества углерода, которое соответствует уравнению
Науглероживание (карбидизацию) проводят в одну или несколько стадий в электрических или реже в газовых печах. Кроме муфельных печей непрерывного действия, применяют угольные трубчатые печи сопротивления, методические печи с молибденовыми нагревателями и вертикальные трехфазные криптоловые печи, а также высокочастотные печи периодического действия с графитовыми тиглями.
В качестве защитного газа используют водород, окись углерода, метан и смеси этих газов. При получении карбидов волфрама и молибдена в качестве защитного газа можно использовать генераторный газ или диссоциированный аммиак.
Реакция науглероживания при образовании монокарбидов протекает по следующим уравнениям:
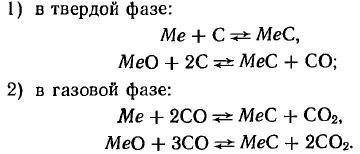
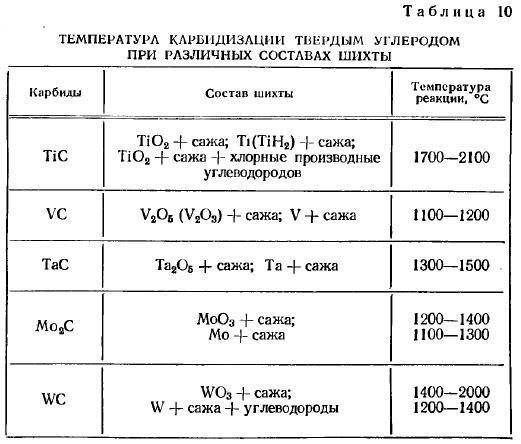
Карбиды молибдена, вольфрама и тантала лучше всего получать науглероживанием металлических порошков сажистым углеродом при температуре 1200—1600°С.
Вольфрам образует два стойких при комнатной температуре карбида: W2C и WC. При науглероживании в твердом состоянии образуется преимущественно монокарбид вольфрама WC, при науглероживании в расплаве образуется W2C. Металлокерамические твердые сплавы содержат исключительно монокарбид вольфрама.
Карбид титана готовят из смеси возможно более чистой двуокиси титана с газовой сажей при температуре 1700—2100° С.
Получение карбидов науглероживанием металловили окислов углеродсодержащими газами. Выше было показано, что при карбидизации в твердом состоянии науглероживание частично происходит и через газовую фазу. В связи с этим возможно получение карбидов науглероживанием исключительно через газовую фазу. Для этого обычно используют металл и углеводород, в результате реакции получают карбид металла и водород. Газовая карбидизация металлов происходит при более высокой температуре.
Науглероживание окислов углеродсодержащими газами проводится редко.
Карбид кальция – это… Что такое Карбид кальция?
Карби́д ка́льция (углеро́дистый ка́льций, ацетилени́д кальция) — CaC2 — в чистом виде белое кристаллическое вещество. Соединение кальция с углеродом.
Получение
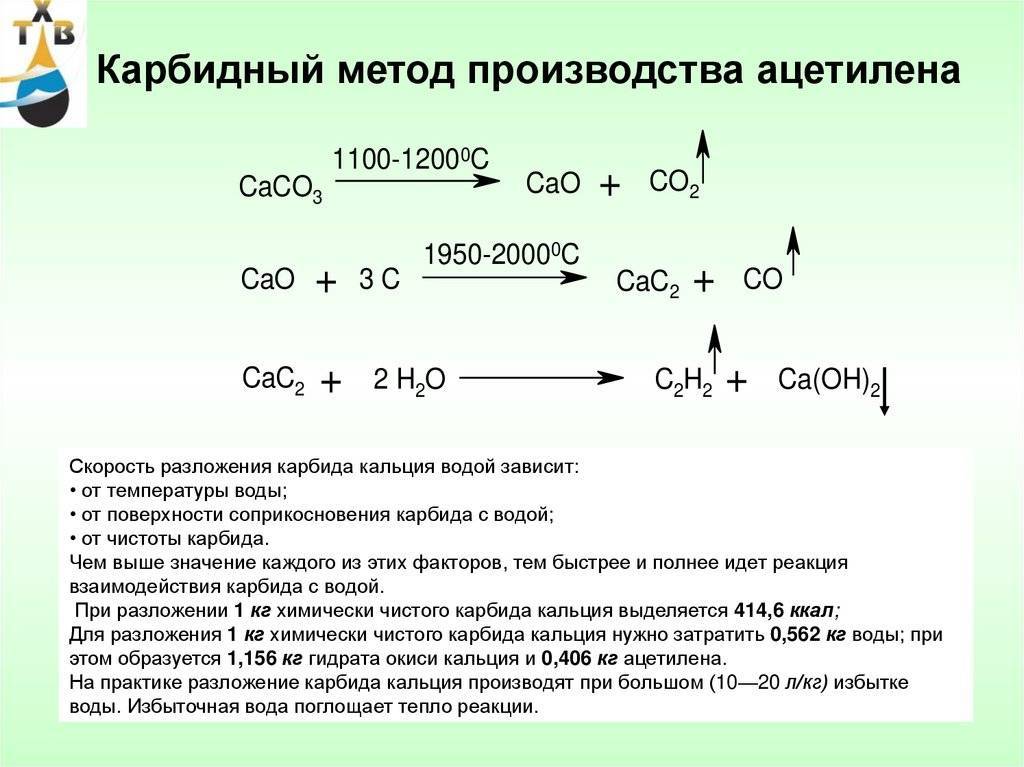
В настоящее время получают прокаливанием в электрических печах (температура 1900—1950 °C) смеси оксида кальция с коксом.
Полученный таким образом технический продукт имеет грязную окраску вследствие загрязнения углём и другими красящими примесями. Он содержит также примеси фосфида и сульфида кальция, вследствие чего такой карбид кальция и полученный из него ацетилен имеют неприятный запах.
Применение
Карбид кальция широко применяют в технике для производства ацетилена, цианамида кальция (при нагревании с азотом), а также для восстановления щелочных металлов.
См. также
| В этой статье не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена. Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники. Эта отметка установлена 31 мая 2011. |
Лабораторный опыт получения ацетилена
Многим из школьных уроков химии знакома реакция взаимодействия карбида с водой. Обычно этот опыт позволяет продемонстрировать реакцию получения ацетилена, а также физические и химические его свойства. Процесс выделения газа при этом происходит достаточно бурно, поэтому трубка, отводящая ацетилен из колбы с действующими веществами, помещается в чашу с водой. Это обеспечивает менее активное и стремительное движение газа. Кроме того, в лабораторных условиях можно использовать и другой способ, чтобы сделать не слишком бурной реакцию разложения такого соединения, как карбид. Ацетилен при этом идет равномерно и спокойно. Для этого вместо воды необходимо взять насыщенный раствор поваренной соли
Также в лаборатории при проведении этой реакции следует осторожно добавлять воду в карбид, помещенный в объемную колбу, а не наоборот
Что такое «карбид», знает любой мальчишка. Если бросить кусочек карбида в лужу, то кроме дикого шипения получается еще дичайшая вонь. А как получается сам карбид?
Вообще карбидов существует множество, как и применений ему. Но нас пока интересует карбид кальция CaC 2 — то есть тот, который используют для получения ацетилена при соединении карбида с водой.
Слишком сложного в получении карбида кальция нет. Сейчас для этого в электропечах пережигают негашеную известь с коксом. При всей этой простоте — впервые карбид кальция был получен в лаборатории в 1836-м году, а промышленно его начали получать в 1892 году. Для попаданца — широчайшее поле для внедрения!
Все реакция — CaO + 3C = CaC 2 + CO Негашеная известь соединяется с углеродом. Негашеную известь получали с древних времен, пережигая известняк, ну и древесный уголь тоже дефицитом не был никогда. Полученный попутно угарный газ (СО) окисляется до углекислого газа прямо при выходе из печи, хотя сейчас часто печи делают закрытыми для сбора угарного газа. На 100 весовых частей негашеной извести нужно 70-80 весовых частей углерода. При производстве лучше иметь избыток угля, чем извести — такой карбид отдает больше ацетилена. Готовый карбид кальция технического качества почти на 80% состоит из самого карбида кальция, 17% — известь, остальное примеси. Карбид выходит в виде расплава, который после затвердевания измельчают.
Но, несмотря на простоту реакции получения, есть некоторые неприятные нюансы. Главное — процесс этот эндотермический, он поглощает дикое количество тепла в процессе производства — 3000 кВт на тонну продукта. Именно из-за этого его делают электродуговым способом. При этом сам процесс идет в жидкой фазе — то есть расплавленная известь постепенно реагирует с кусками углерода. При этом нужна температура примерно 2000°С, что совсем немало. И что совсем неприятно — при перегреве до 2200-2400°С карбид кальция распадается на составляющие.
Поэтому, если нам не доступно электричество в больших объемах, у нас есть два выхода.
Первый — это плавить в тигле. Проблема в том, что тигель должен выдержать эти самые 2000°С, а в древние времена ни графитовый, ни вольфрамовый тигель нам будут недоступны.
Второй — построить небольшую доменную печь. Требуемое тепло даст избыточное количество угля. Уголь и известь насыпаются туда слоями и печь поддувается большим количеством воздуха. Такие печи пытались строить и главная проблема — поддержка точных условий реакции, что регулируется силой поддува. С одной стороны — такую печь можно построить только когда уже работают доменные печи для железа. А с другой стороны — а нам точно нужен карбид, если нет даже железа?
Трудность вызовет хранение карбида. Он должен быть абсолютно изолирован от воды — много лучше, чем порох. Потому что если порох намокнет, то он не взорвется, а если намокнет карбид — то взрыв обеспечено. И что хуже всего — при хранении не должна использоваться медь, серебро или золото.
Проблем с производством карбида будет немало. Но при каком производстве их будет мало? Зато все проблемы — решаемые чуть ли не с технологиями Древнего Египта. А пользы от карбида будет много…
И последнее — ацетилен, который получается после контакта карбида с водой — ничем не пахнет, человек просто не имеет обонятельных рецепторов для него. Та вонь, по которой мы безошибочно определяем карбид — это примеси, которых в техническом карбиде несколько процентов.
Техника безопасности при работе с карбидом кальция.
Как уже Вам известно, карбид кальций – это взрывоопасное вещество и для обеспечения безопасной работы с ним необходимо выполнять несколько обязательных правил при использовании карбида для сварки. Главные положения, которые необходимо выполнять при сварочных работах на основе карбида кальция:
Учитывайте, что карбид кальция активно взаимодействует с воздухом и водой, выделяя легковоспламеняющийся ацетиленовый газ
Место хранения карбида для сварки должно быть сухим и герметичным.
Карбид кальция также взрывоопасен, поэтому искры и открытый огонь рядом с веществом строго воспрещены.
Пыль карбида (куски менее 2 мм) вызывают раздражения, попадая на кожу, глаза и слизистую оболочку рта, и носа.
Регулярные сварочные работы с применением карбида кальция должны проводиться в специально оборудованном для сварки помещении, в котором нет горючих веществ, и присутствуют только несгораемые материалы
Жизненно важно, чтобы все оборудование, связанное с хранением и производством ацетилена было изолировано в отдельных отсеках сварочной мастерской, а само помещение для генераторов должно легко проветриваться и в случае чего деактивироваться.
Установка генераторов ацетилена строго запрещена в подвальных комнатах.
После завершения сварочных работ с применением карбида кальция как «топлива», в генераторах все оставшееся вещество дорабатывается, и полученные шлаки в виде известкового ила удаляем из генератора в специальную яму или бункер.
Напомним, что карбид и ацетилен – взрывоопасные вещества. Поэтому курение, открытый огонь на расстоянии до 10 метров от места хранения отработанного карбида строго воспрещено.
При перевозке и хранении ацетиленовых баллонов, на конструкцию клапанов должны быть навинчены предохранительные колпаки
Толчки и удары при транспортировке нескольких баллонов смертельно опасны. Хранение и перевозка ацетиленовых баллонов с другими веществами не допустима.
И напоследок отметим, что карбид кальция является высокоинтенсивным веществом для получения ацетиленового газа, что сводит к минимуму его расход. Кроме того, один килограмм ацетилена, полученного из карбида кальция, выделяет тепла около 8 тысяч кДж.
использовать
В просторечии карбид обычно приравнивается к карбиду кальция . В газогенераторе он реагирует с водой с образованием этина (обычное название: ацетилен), который используется для различных целей.
- В прошлом карбид кальция смешивался с водой в карбидных лампах , с которой он реагировал с образованием горючего этина ; этин был зажжен и горел ярким пламенем. Этот метод использовался, в частности, в шахтных светильниках при подземных горных выработках. Спелеологи по-прежнему отдают предпочтение карбидным лампам, потому что они дают особенно красивый свет, а пламя можно использовать для обозначения поверхностей сажей .
- Производство цианамида кальция
- Синтез этина, работа карбидных проявителей (сегодня актуально только в развивающихся странах)
- Для обессеривания чугуна и жидкой стали в сталелитейной промышленности.
- Примерно с 1900 года до 1930-х годов карбидные лампы, специально изготовленные для этой цели, также использовались в качестве велосипедных фонарей. Эти карбидные велосипедные фонари светят намного ярче, чем соответствующие масляные или свечные лампы.
- Образование этина используется для определения остаточной влажности образцов почвы или бетона . Здесь образец заполняется в стандартизированную стальную бутылку вместе с ампулой карбида кальция и четырьмя стальными шариками и герметизируется головкой манометра. Бутылку встряхивают, в результате чего образец дробится, а ампула с карбидом кальция разбивается. Давление газа, возникающее в результате реакции карбида кальция и влаги, можно считать на головке манометра и преобразовать в содержание влаги. Этот процесс известен как карбидный метод (CM) . Метод используется, например, после того, как стяжка была уложена, чтобы определить, можно ли уже укладывать верхнее покрытие.
- Карбид кальция используется в качестве активного ингредиента в репеллентах для отпугивания полевок и кротов . Газовая смесь, возникающая при контакте с почвенной влагой, отгоняет животных, не убивая их.
Карбидная стрельба
→ Основная статья : Твердосплавные заклепки
Если положить несколько кусочков карбида кальция в молочную банку и сбрызнуть их небольшим количеством воды, в объеме, закрытом крышкой или футбольным мячом , образуется взрывоопасная газовая смесь этина и кислорода . Затем газовая смесь воспламеняется через предварительно просверленное отверстие в земле. Взрыв может отбросить крышку или футбольный мяч на расстояние до 70 м. В отличие от картофельной пушки , направление менее предсказуемо. Традиция стрельбы из карбида в основном культивируется в Нидерландах, а также в некоторых частях северо-западной Германии и северной Баварии молодыми людьми на свадьбах, в канун Нового года и Новый год. В Верхней Лужице это называют пасхальной стрельбой . В восточно-фризской области Германии и восточной части Нидерландов стрельба из карбида является неотъемлемой частью традиционных празднований Нового года. В Каринтии (Австрия) стрельба из карбида проводится по пасхальному обычаю – от благословения еды в Великую субботу до празднования воскресения утром в пасхальное воскресенье.
Карбидная рыбалка
Во время голода после Второй мировой войны многие люди использовали тот же принцип , чтобы иметь возможность быстро и вычистить много рыбы, взорвав твердосплавную банку, которая в то время была легко доступна в рыбных водах , несмотря на запрет динамитная рыбалка .
Топливный газ для сварки
Карбид широко использовался примерно до 1960 года для получения высокоэнергетического топливного газа ацетилена (этина) в проявителях карбида при низком давлении, который – в сочетании с кислородом – уникально хорош для сварки ( сварка плавлением газа ) стали. благодаря своей особенно высокой температуре пламени ( железные сплавы ), например, подходит для производства трубопроводов в секторе газа / воды / отопления. Большие газовые генераторы постоянно устанавливались в мастерских, а меньшие – на строительных площадках. Для этого карбид нужно было хранить в жестяных банках, например, защищенных от попадания водяного пара.
Этот процесс производства ацетилена на месте был необходим, потому что ацетилен, если его сжать для хранения в обычном газовом баллоне, разложился бы с серьезными последствиями и в то же время выделил бы тепло.
Только с техническим развитием ацетиленового баллона , в котором этот газ может безопасно храниться в растворенном виде в растворителе под средним или высоким давлением, подача газа может быть переключена на баллоны и упрощена для пользователя. В течение долгого времени бутылки с ацетиленом содержали канцерогенный асбест, они все еще тяжелые и чувствительны к ударам и нагреванию из-за растворителей и пористой подложки.
Где взять карбид?
Поместите посуду над спиртовкой или газовой горелкой. Выпаривайте раствор на медленном огне до получения кристаллического нитрата кальция. Будьте осторожны при работе с кислотой. Работайте в перчатках и защитных очках. Используйте только достаточно разбавленную азотную кислоту, чтобы исключить слишком быстрое прохождение реакции. Храните нитрат кальция в герметично закрытых емкостях. Он очень гигроскопичен и быстро набирает влагу из воздуха. Ацетилен – самый простой представитель класса алкинов, имеет химическую формулу С2Н2. Бесцветный газ, горюч, в смеси с воздухом взрывоопасен. Благодаря наличию тройной связи в своей молекуле, весьма активен с химической точки зрения, легко вступает в реакции присоединения. При сгорании выделяет большое количество тепла, что может быть использовано, например, многим известная «ацетиленовая горелка». Как же его синтезировать?  При хранении ацетилена следует учитывать его особенности. Например, его нельзя держать в баллонах, имеющих бронзовый вентиль, поскольку газ реагирует с медью, входящей в состав бронзы, образуя чрезвычайно взрывоопасное вещество – ацетиленид меди. Самый старый, проверенный временем метод получения ацетилена – реакция карбида кальция с водой. Наверное, многие мальчишки в детстве развлекались, бросая кусочки карбида в лужу, тут же начиналось яростное шипение, карбид буквально «бурлил», исчезая на глазах, и в воздухе отчетливо пахло чем-то резким, «острым». Эта реакция протекает таким образом: СаС2 + 2Н2О = С2Н2 + Са(ОН)2 Для того чтобы она протекала не слишком бурно, можно использовать не простую воду, а насыщенный раствор хлорида натрия, например. Если этот опыт планируется показать на уроке химии, следует подобрать реакционную колбу подходящего размера. Если она будет слишком маленькой, то образующая при растворении карбида пена может быть «выброшена» давлением ацетилена в отводную трубку, и дальше – в приемный сосуд. В случае же с чересчур большой колбой, придется долго ждать, пока образующийся ацетилен не вытеснит весь воздух из прибора. Воду, а лучше насыщенный раствор хлорида натрия, следует добавлять в колбу с кусочками карбида медленно, по каплям, регулируя скорость реакции, не допуская, чтобы она протекала чересчур бурно. Используется ацетилен в самых разных областях. Например, как сырье для получения целого ряда химических веществ (уксусной кислоты, пластмасс, некоторых ароматических углеводородов, некоторых видов синтетического каучука, этилового спирта и т.д.). На его основе синтезируют некоторые очень сильные взрывчатые вещества, используемые в качестве инициаторов, т.е. для детонации. Повсеместно применяется при резке и сварке металлов, при получении яркого света в автономных светильниках. Электрическая дуга – явление очень яркое, поэтому используйте темные очки, берегите глаза. При приготовлении смеси не обязательно считать молярную массу, просто старайтесь брать кокс в избытке, дело в том, что в процессе лишний углерод выгорит на воздухе. Чем больше ток, тем лучше, но без фанатизма. Как получить карбид кальция
При хранении ацетилена следует учитывать его особенности. Например, его нельзя держать в баллонах, имеющих бронзовый вентиль, поскольку газ реагирует с медью, входящей в состав бронзы, образуя чрезвычайно взрывоопасное вещество – ацетиленид меди. Самый старый, проверенный временем метод получения ацетилена – реакция карбида кальция с водой. Наверное, многие мальчишки в детстве развлекались, бросая кусочки карбида в лужу, тут же начиналось яростное шипение, карбид буквально «бурлил», исчезая на глазах, и в воздухе отчетливо пахло чем-то резким, «острым». Эта реакция протекает таким образом: СаС2 + 2Н2О = С2Н2 + Са(ОН)2 Для того чтобы она протекала не слишком бурно, можно использовать не простую воду, а насыщенный раствор хлорида натрия, например. Если этот опыт планируется показать на уроке химии, следует подобрать реакционную колбу подходящего размера. Если она будет слишком маленькой, то образующая при растворении карбида пена может быть «выброшена» давлением ацетилена в отводную трубку, и дальше – в приемный сосуд. В случае же с чересчур большой колбой, придется долго ждать, пока образующийся ацетилен не вытеснит весь воздух из прибора. Воду, а лучше насыщенный раствор хлорида натрия, следует добавлять в колбу с кусочками карбида медленно, по каплям, регулируя скорость реакции, не допуская, чтобы она протекала чересчур бурно. Используется ацетилен в самых разных областях. Например, как сырье для получения целого ряда химических веществ (уксусной кислоты, пластмасс, некоторых ароматических углеводородов, некоторых видов синтетического каучука, этилового спирта и т.д.). На его основе синтезируют некоторые очень сильные взрывчатые вещества, используемые в качестве инициаторов, т.е. для детонации. Повсеместно применяется при резке и сварке металлов, при получении яркого света в автономных светильниках. Электрическая дуга – явление очень яркое, поэтому используйте темные очки, берегите глаза. При приготовлении смеси не обязательно считать молярную массу, просто старайтесь брать кокс в избытке, дело в том, что в процессе лишний углерод выгорит на воздухе. Чем больше ток, тем лучше, но без фанатизма. Как получить карбид кальция
Применение карбида кальция
Как ранее было отмечено, карбид кальция встречается в самых различных областях промышленности, зачастую поставляют для проведения промышленного синтеза. Свойства карбида кальция и реакция, протекающая при его соединении с различными веществами, определяют использование вещества в нижеприведенных случаях:
- Многие синтетически компоненты, входящих в состав современных материалов, производят на основе рассматриваемого компонента.
- Применяется для получения цианамида кальция. Подобный компонент используется для получения различных химических удобрений. Именно поэтому сырье применяется для регулирования скорости роста растений.
- Цианамид кальция также получают при соединении вещества с азотом.
- В некоторых случаях проводится восстановление металлов щелочной группы.
- Можно использовать рассматриваемое соединение в процессе газовой сварки.
При рассмотрении карбида кальция и области применения стоит учитывать, что подобное вещество чаще всего применяют для получения ацетилена. Подобный синтез карбида кальция разработал немецкий ученый. Среди особенностей подобного способа применения отметим следующие моменты:
- Ацетилен из карбида получают при оказании воздействия водой на используемое сырье.
- В результате прохождения химической реакции образуется требующийся газ, гашеная известь выпадает в осадок.
- Стоит учитывать, что при смешивании компонентов выделяется большое количество тепла. Поэтому работа должна проводится с учетом техники безопасности.
- В зависимости от вида применяемой технологии переработки сырья с 1 килограмма выходит около 290 литров газа.
- Скорость протекания процедуры зависит от чистоты применяемого сырья, температуры и количества воды.

Получение ацетилена из карбида кальция
Как показывает практика, при использовании чистого карбида на протекание химической реакции отводится около 20 литров волы на 1 килограмм сырья. Подобное количество воды требуется для того чтобы снизить температуру реакции, за счет чего обеспечиваются оптимальные условия для работы.
Индивидуальные доказательства
- ↑ Запись о В: Römpp Online . Георг Тиме Верлаг, доступ 10 ноября 2014 г.
- ↑ техническое (PDF) от Карла Рота , по состоянию на 14 декабря 2010 г.
- ↑ запись на в базе данных GESTIS субстанцию на выставке IFA , доступ к 1 февраля 2016 года. (Требуется JavaScript)
- Дэвид Р. Лид (Ред.): Справочник по химии и физике CRC . 90-е издание. (Интернет-версия: 2010 г.), CRC Press / Тейлор и Фрэнсис, Бока-Ратон, Флорида, Стандартные термодинамические свойства химических веществ, стр. 5-20.
- М. Бинньюис и другие: Allgemeine und Anorganische Chemie . 2-е издание. Спектр, 2010, ISBN 3-8274-2533-6 , стр.383 .
- ↑ Георг Брауэр (ред.), В сотрудничестве с Марианн Бодлер и другими: Справочник по препаративной неорганической химии. 3-е, переработанное издание. Том II, Фердинанд Энке, Штутгарт 1978, ISBN 3-432-87813-3 , стр. 931-932.
- Зигфрид Хауптманн : Органическая химия , 2-е издание, VEB Deutscher Verlag für Grundstoffindindustrie, Лейпциг 1985, ISBN 3-342-00280-8 , стр. 263.
Сварка карбидом
Сварка карбида, сделанного на основе кремния, подразумевает его непосредственный контакт с водой, в ходе которого выделяется значительное количество ацетиленового газа и много тепла. Из-за данной эксплуатационной характеристики обеспечить безопасное хранение данного материала не так-то просто. Для того чтобы это сделать, карбид кладут в абсолютно герметичные баки, выполненные из кровельного металла. В них должно помещаться от 100 до 130 кг.
При сварке карбидом выделяется большое количество ацетилена — газа, отличающегося быстрой воспламеняемостью, поэтому при открытии таких бидонов следует позаботиться, чтобы поблизости не было искр и открытого пламени.
Сварочные работы с использованием карбидной пыли с размером частиц 2 мм и менее производиться не будут, так как такая пыль практически моментально растворяется в воде. Если же добавить в воду слишком большое количество такой пыли, то существует реальная вероятность взрыва. Между прочим, килограмм карбида может привести к выделению почти целого кубометра чистого ацетилена.
Карбид весьма широко используется для сварки газового типа, а также для резки металлов. Когда ацетилен начинает гореть вместе с кислородом, температура пламени может достигать свыше 3000 градусов по Цельсию. Это позволяет применять данный материал даже при работе с тугоплавкими материалами.
Какие меры безопасности нужны при работе с карбидом?
Выше говорилось, что карбид является взрывоопасным веществом, поэтому следует соблюдать определенные правила, которые помогут не допустить получения травм:
- Это вещество практически моментально вступает во взаимодействие с воздухом и водой, причем результатом данной химической реакции будет горючий ацетилен. Вследствие такого свойства карбида для сварки его следует хранить в абсолютно сухой и герметичной таре.
- Взрывоопасен не только выделяющийся газ, но и сам карбид, поэтому поблизости него не должно находиться искр или открытого пламени.
- Карбидная пыль с размером частиц менее 2 мм при попадании на кожу и глаза может вызвать раздражение, поэтому работать с материалом следует в защитных перчатках и в очках.
- Постоянная сварка с использованием карбида производится только в специальном помещении, где отсутствуют горючие вещества, а все предметы, находящиеся там, должны быть абсолютно несгораемыми. Хранить оборудование следует в полностью изолированных отсеках помещения. В нем должна быть оборудована система принудительной вентиляции.
- Генераторы ацетилена, использующие в своей работе карбид, категорически запрещено размещать в подвальных помещениях.
- Когда работы, связанные с проведением сварки, будут завершены, все загруженное вещество нужно будет выработать. Отработанные шлаки (они, как правило, представляют собой известковый налет) удаляются в бункер или в иное специально отведенное под это место.
- Нельзя курить поблизости от проведения работ, рядом с самим карбидом — использование открытого огня разрешено на расстоянии не менее 10 метров.
- Когда осуществляется транспортировка или хранение баллонов с ацетиленом, на клапаны в обязательном порядке надеваются защитные колпачки, также во время перевозки нельзя допускать соударения баллонов или тем более их падения. Производить транспортировку вместе с другими веществами также запрещено.
Как правильно применять карбид для проведения сварных работ?
Технология использования этого материала представляет собой следующую последовательность действий:
- Его куски укладывают в корзину, причем их величина не должна превышать 8 см в диаметре, так как такой размер позволяет обеспечить выделение наибольшего количества ацетилена. Всю карбидную пыль предварительно удаляют, чтобы не допустить детонации материала во время работ.
- В аппарат, заполненный водой, устанавливают эту корзину, тщательно закрывая ее специальной крышкой, оснащенной винтом поперечной подачи.
- Начинают аккуратно вращать маховик винта, чтобы корзина постепенно опустилась в воду. Резкого погружения не допускают, так как это может привести к воспламенению газа и последующему взрыву. Карбид начнет постепенно реагировать с водой, выделяя значительные объемы ацетилена.
С того момента, как началось выделение ацетилена, можно приступать к проведению сварочных работ. Используют карбид для сварки стали, нержавеющих материалов, цветных металлов, а также разного рода заготовок, отличающихся достаточно высокой температурой плавления. В разобранном виде установка для ацетиленовой сварки является абсолютно безопасной. electrod.biz