Почему CO2 в аквариуме – дефицит?
Посмотрите на биотоп любого природного пресного водоёма. Водных растений там обычно немного, и сидят они редко, а дно покрыто органическими отложениями, в которых в изобилии живут разнообразные микро- и макроорганизмы, в основном беспозвоночные. Да и рыбы изрядно, и головастиков… И все они – от микроорганизмов, перерабатывающих донные отложения, до рыбы и лягушек, выделяют в воду значительные количества СО2. Иное дело – типичный растительный аквариум, который, как правило, густо засажен растениями, а рыбы в нём мало, и она невелика (ибо большинство крупных рыб портят растения). Обычное население наших аквариумов – мелкая стайная харацинка и гуппи с пецилиями, которые в силу малого размера и медленного обмена веществ углекислого газа выделяют совсем мало.
А вот света в наших обычных аквариумах в достатке, азота с фосфором – обычно тоже хватает. Вот и получается, что тем самым «лимитирующим фактором» становится СО2. Часть растений при его дефиците просто угнетаются в росте и в конце концов погибает, а другие – приспособились сами добывать себе СО2 из минеральных веществ, разлагая растворённые в любой воде гидрокарбонаты. При этом в качестве «побочного продукта» образуются нерастворимые соли кальция, выпадающие на листьях таких растений в виде грубой некрасивой корки (на которой быстро поселяются одноклеточные диатомовые водоросли). Такой фокус умеют проделывать элодеи, анубиасы, роголистники и некоторые другие виды, живущие в природе в стоячих водоёмах и сталкивающиеся там с периодическим дефицитом углекислоты. Так что если мы хотим, чтобы растения выглядели так, как на картинках в интернете, а не являли из себя тощие унылые и понурые хвостики, покрытые известковой коркой и водорослевыми обрастаниями, то волей-неволей придётся подумать о добавлении в аквариум углекислого газа.
Если же вы привыкли более дотошно подходить к таким проблемам, и мои краткие пояснения вас не убедили – советую обратиться к научной статье вот по этой ссылке, в которой всё это подробно разъяснено с точки зрения химии и биохимии:
- Углекислый газ и карбонатная система воды. Часть 1.
- Углекислый газ и карбонатная система воды. Часть 2.
Мы же перейдём к практике. Но прежде – маленькое предупреждение:
Углекислый газ: получение в промышленности
Существует большое количество способов промышленного получения углекислоты. Наиболее рентабельными являются варианты добычи газа, основанные на получении СО2, который образовывается на химических производствах в виде отходов.
Газообразный оксид углерода (IV) получают из промышленного дыма способом адсорбции моноэтаноламина. Частицы этого вещества подаются в трубу с отходами и вбирают в себя углекислоту. После прохождение через смесь CO2 моноэтаноламины направляются на очистку в специальные резервуары, в которых, при определённых показателях температуры и давления, происходит высвобождение углекислого газа.
Углекислый газ высокого качества получается в результате брожения сырья при изготовлении спиртных напитков. На таких производствах газообразный СО2 обрабатывают водородом, перманганатом калия и углем. В результате реакции получают жидкую форму углекислоты.
Твёрдое состояние СО2 или «сухой лёд» также получают из отходов пивоваренных заводов и ликероводочных производств. Это агрегатное состояние вещества в промышленных масштабах образуется в такой последовательности:
- Из резервуара, где происходит брожение, газ подаётся в ёмкость для промывки.
- Углекислота направляется в газгольдер, в котором подвергается воздействию повышенного давления.
- В специальных холодильниках СО2 охлаждается до определённой температуры.
- Образовавшаяся жидкость фильтруется через слой угля.
- Углекислота снова направляется в холодильник, где производится дополнительное охлаждение вещества с последующим прессованием.
Таким образом получается высококачественный «сухой лёд», который может использоваться в пищевой промышленности, растениеводстве или в быту.
Монооксид углерода
Угарным газом называют оксид углерода с формулой CO. Кроме того, это соединение называют монооксидом и окисью углерода. Он представляет собой бесцветный безвкусный горючий газ без запаха, который легче воздуха. Вещество образуется в случаях, когда топливо сгорает не до конца. Оно плохо растворяется в воде.
У молекулы этого оксида линейное строение. Между атомами его элементов образуется тройная связь. Два неспаренных электрона обоих элементов образуют пару ковалентных связей. Третья же связь возникает, когда электронная пара кислорода размещается на свободной орбитали атома углерода.
Химические свойства
Оксид углерода (II) не образует солей и является восстановителем. Кроме того, к химическим свойствам угарного газа относятся:
- Горение синим пламенем в кислородной атмосфере.
- Окисление хлором, если присутствует катализатор или на него воздействует свет. При этом образуется ядовитое газообразное вещество — фосген. Молекулярное уравнение реакции: CO + Cl2 → COCl2.
- При повышенном давлении вещество вступает во взаимодействие с водородом. Из этой смеси, называемой синтез-газом, при различных условиях получают углеводороды, например, метан.
- При наличии давления оксид углерода (II) вступает в реакцию с щелочами. В результате появляется соль муравьиной кислоты.
- Восстановление металлов из оксидов. К примеру, взаимодействие с оксидом железа (III) даёт железо и углекислый газ.
- Реакции с сильными окислителями приводят к образованию углекислого газа или карбонатов.
Способы изготовления
Получить монооксид можно как в лабораторных условиях, так и в производственных. В первом случае для образования необходимого вещества используют концентрированную серную и муравьиную или щавелевую кислоты.
В промышленности для получения угарного газа применяют специальные газогенераторы. В них соединение вырабатывается воздухом, проходящим через раскалённый уголь. Ещё одним промышленным методом изготовления газа является паровая конверсия метана или угля. Кроме того, на производстве используют процесс неполного окисления метана.
Угарный газ присутствует и в атмосфере планеты. Он туда поступает тремя способами:
- неполное разложение органических веществ без доступа воздуха;
- сгорание биологической массы, например, лесные и степные пожары;
- выхлопные газы, которые образуются в двигателях внутреннего сгорания.
Использование соединения
Основное применение горючего вещества — изготовление генераторного или воздушного газа, для чего монооксид смешивают с азотом. Кроме того, соединяя его с водородом, получают водяной газ.
Влияние на живые организмы
Монооксид крайне токсичен, потому что связывается с находящимся в крови гемоглобином прочнее и во много раз быстрее кислорода. Он блокирует процессы доставки жизненно необходимого вещества.
Если концентрация вещества в атмосфере превышает 0,1%, то живые организмы погибают в течение одного часа. Если же уровень оксида этого типа поднимается до 0,3%, то смерть наступает в течение нескольких минут. По этим причинам угарный газ относится к быстродействующим отравляющим веществам.
Специалистами установлено, что чаще всего люди погибают при пожарах в результате отравления указанным углеродным соединением, поскольку он является неотъемлемым продуктом горения большинства материалов. Кроме того, оксид вырабатывается двигателями автомобилей, что также приводит к гибели неосторожных граждан, например, механиков, которые пренебрегают организацией должной вентиляции в гараже.
Если отравление лёгкой степени, то пострадавшему для восстановления здоровья будет достаточно гипервентиляции лёгких кислородом. Если же отравление тяжёлое, то человеку потребуется серьёзная медицинская помощь.
Углекислый газ: хранение и транспортировка
Хранение СО осуществляется в баллонах чёрного цвета, на корпусе которых обязательно должна быть надпись «Углекислота».
Кроме этого, на ёмкости наносится маркировка, по которой можно получить информацию о производителе баллона, весе пустой ёмкости, а также узнать дату последнего освидетельствования. Нельзя использовать углекислотные баллоны, у которых:
- Истёк срок освидетельствования.
- Имеются повреждения.
- Неисправны вентили.
Транспортировка наполненных газом баллонов должна осуществляться по следующим правилам:
- Транспортировать ёмкости только в горизонтальном положении. Вертикальное размещение допускается только в том случае, если имеются специальные ограждения, которые препятствуют падению баллона во время перевозки.
- Для безопасного перемещения на баллонах должны быть резиновые кольца.
- Не допускать механических воздействий, а также чрезмерного нагрева.
- Запрещается перевозка углекислотных баллонов в торговых аппаратах.
Кроме этого, техникой безопасности запрещается переносить баллоны вручную или перекатывать их по земле.
Хранение баллонов с углекислотой может осуществляться как в специально оборудованных помещениях, так и под открытым небом. В зданиях ёмкости следует размещать на расстоянии не менее 1 метра от отопительных приборов. При хранении на улице необходимо оградить ёмкости от воздействия прямых солнечных лучей и осадков, поэтому размещать резервуары таким способом рекомендуется под навесом. Если хранение баллонов осуществляется в неотапливаемом помещении или под открытым небом, то в зимнее время необходимо следить за тем, чтобы ёмкости не охлаждались ниже минус 40 градусов Цельсия.
Ваша оценка?
Мне нравитсяНе нравится
Применение диоксида углерода
Пищевая промышленность после масштабного получения «сухого льда» перешла на принципиально новый метод хранения продуктов. Он незаменим при производстве газированных напитков и минеральной воды. Содержание СО2 в напитках придает им свежесть и заметно увеличивает срок хранения. А карбидизация минеральных вод позволяет избежать затхлости и неприятного вкуса.
В кулинарии часто используют метод погашения лимонной кислоты уксусом. Выделяющийся при этом углекислый газ придает пышность и легкость кондитерским изделиям.
Данное соединение часто используется в качестве пищевой добавки, повышающей срок хранения пищевых продуктах. Согласно международным нормам классификации химических добавок содержания в продуктах, проходит под кодом Е 290,
Порошкообразный углекислый газ – одно из наиболее популярных веществ, входящих в состав пожаротушительных смесей. Это вещество встречается и в пене огнетушителей.
Транспортировать и хранить углекислый газ лучше всего в металлических баллонах. При температуре более 31⁰С давление в баллоне может достигнуть критического и жидкий СО2 перейдет в сверхкритическое состояние с резким подъемом рабочего давления до 7,35 МПа. Металлический баллон выдерживает внутреннее давление до 22 МПа, поэтому диапазон давления при температурах свыше тридцати градусов признается безопасным.
Углекислый газ, формула, молекула, строение, состав, вещество:
Углекислый газ (диоксид углерода, двуокись углерода, углекислота, оксид углерода (IV), угольный ангидрид) – бесцветный газ, почти без запаха (в больших концентрациях с кисловатым «содовым» запахом).
Углекислый газ – бинарное химическое соединение углерода и кислорода, имеющее формулу CO2.
Химическая формула углекислого газа CO2.
Строение молекулы углекислого газа, структурная формула углекислого газа:
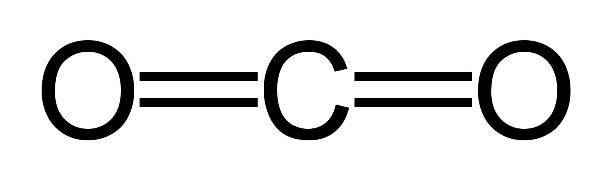
Углекислый газ тяжелее воздуха приблизительно в 1,5 раза. Его плотность при нормальных условиях составляет 1,98 кг/м3, по отношении к воздуху – 1,524. Поэтому скапливается в низких непроветриваемых местах.
Концентрация углекислого газа в воздухе (в атмосфере Земли) составляет в среднем 0,046 % (по массе) и 0,0314 % (по объему).
Углекислый газ вырабатывается в органах и тканях человека образуется в качестве одного из конечных продуктов метаболизма. Он переносится от тканей по венозной системе и затем выделяется с выдыхаемым воздухом через лёгкие. Таким образом, содержание углекислого газа в крови велико в венозной системе, уменьшается в капиллярной сети лёгких, и содержание его мало в артериальной крови. В выдыхаемом человеком воздухе содержится около 4,5% диоксида углерода, что в 60-110 раз больше, чем во вдыхаемом. Организм человека выделяет приблизительно 1 кг углекислого газа в сутки.
Углекислый газ растворяется в воде. В 100 граммах воды растворяется 0,3803 грамма CO2 при 16 °C, 0,3369 грамма CO2 – при 20 °C, 0,2515 грамма CO2 – при 30 °C. Растворяясь в воде, образует угольную кислоту Н2CO3. Растворим также в ацетоне, бензоле, метаноле и этаноле.
Термически устойчив при температурах менее 1000 °C. При температуре 1000 °C восстанавливается углем до оксида углерода (II).
При нормальном атмосферном давлении диоксид углерода не существует в жидком состоянии, существует только в твердом или газообразном состоянии. Твердая двуокись углерода при повышении температуры не плавится, а переходит (возгоняется) непосредственно из твёрдого состояния в газообразное. Твёрдую двуокись углерода также называют сухим льдом. Внешний вид сухого льда напоминает обычный лед, снегоподобную массу. При сублимации сухой лед поглощает около 590 кДж/кг (140 ккал/кг) теплоты.
Под давлением 35 000 атм. твердая углекислота становится проводником электрического тока.
Жидкий углекислый газ можно получить при повышении давления. Так, при температуре 20 °С и давлении свыше 6 МПа (~60 атм.) газ сгущается в бесцветную жидкость. При нормальных условиях (20 °С и 101,3 кПа) при испарении 1 кг жидкой углекислоты образуется 509 л углекислого газа. Хранят и транспортируют углекислый газ, как правило, в жидком состоянии
Двуокись углерода негорюча, но в ее атмосфере может поддерживаться горение активных металлов, например, щелочных металлов и щелочноземельных – магния, кальция, бария.
Двуокись углерода нетоксична, невзрывоопасна.
Предельно допустимая концентрация двуокиси углерода в воздухе рабочей зоны не установлена, при оценке этой концентрации можно ориентироваться на нормативы для угольных и озокеритовых шахт, установленные в пределах 0,5% (об.) или 9,2 г/м (см. ГОСТ 8050-85 «Двуокись углерода газообразная и жидкая. Технические условия»).
По степени воздействия на организм человека двуокись углерода относится к 4-му классу опасности по ГОСТ 12.1.007-76.
При концентрациях более 5% (92 г/м) двуокись углерода оказывает вредное влияние на здоровье человека, так как она тяжелее воздуха в полтора раза и может накапливаться в слабопроветриваемых помещениях у пола и в приямках, а также во внутренних объемах оборудования для получения, хранения и транспортирования газообразной, жидкой и твердой двуокиси углерода. При этом снижается объемная доля кислорода в воздухе, что может вызвать явление кислородной недостаточности и удушья.
Углекислый газ образуется при гниении и горении органических веществ, в результате вулканической деятельности. Содержится в воздухе и минеральных источниках, выделяется при дыхании животных и растений. Искусственными источниками образования углекислого газа являются промышленные выбросы и выхлопные газы автомобильного транспорта.
Углекислый газ легко пропускает излучение в ультрафиолетовой и видимой частях спектра, которое поступает на Землю от Солнца и обогревает её. В то же время он поглощает испускаемое Землёй инфракрасное излучение и является одним из парниковых газов, вследствие чего участвует в процессе глобального потепления.
Свойства токсичного вещества
В природе и свойствах угарного газа нет ничего необычного. По сути, это продукт частичного окисления угля или угольсодержащих видов топлива. Формула угарного газа проста и незамысловата – СО, в химических терминах — монооксид углерода. Один атом углерода соединен с атомом кислорода. Так уж устроена природа процессов горения органического топлива, что угарный газ является неотъемлемой частью любого пламени.
Угли, родственные им виды топлива, торф, дрова при нагреве в топке газифицируются в угарный газ, и только потом дожигаются притоком воздуха. Если угар просочился из камеры горения в помещение, то он будет оставаться в стабильном состоянии до момента, когда вентиляцией угарный поток будет вынесен из комнаты или накапливаться, заполняя все пространство, от пола до потолка. В последнем случае спасти положение может только электронный датчик угарного газа, реагирующий на малейшее повышение концентрации токсичного угара в атмосфере помещения.
Что необходимо знать об угарном газе:
- В стандартных условиях плотность угарного газа – 1,25 кг/м3, что очень близко к удельному весу воздуха 1,25 кг/м3. Горячий и даже теплый монооксид легко поднимается под потолок, по мере остывания оседает и перемешивается с воздухом;
- Угарный газ не имеет вкуса, цвета и запаха, даже в условиях высокой концентрации;
- Для начала образования угарного газа достаточно нагреть металл, контактирующий с углеродом, до температуры в 400-500оС;
- Газ способен гореть в воздухе с выделением большого количества тепла, примерно 111 кДж/моль.
Опасно не только вдыхание угарного газа, газовоздушная смесь способна взрываться при достижении объемной концентрации от 12,5% до 74%. В этом смысле газовая смесь похожа на бытовой метан, но гораздо опаснее сетевого газа.
Метан легче воздуха и менее токсичен при вдыхании, кроме того, благодаря добавке в газовый поток специальной присадки – меркаптана, его наличие в помещении легко уловить по запаху. При небольшой загазованности кухни можно без последствий для здоровья войти в помещение и проветрить его.
С угарным газом все сложнее. Близкое родство СО и воздуха препятствует эффективному удалению токсичного газового облака. По мере охлаждения облако газа будет постепенно оседать в области пола. Если сработал датчик угарного газа, или обнаружилась утечка продуктов горения из печи или котла на твердом топливе, необходимо немедленно принимать меры к проветриванию, иначе первыми пострадают дети и домашние питомцы.
Подобное свойство угарного облака ранее широко использовалось для борьбы с грызунами и тараканами, но эффективность газовой атаки значительно ниже современных средств, а риск заработать отравление несоизмеримо выше.
При наличии подозрения в накоплении угарного газа в подвальных помещения, подсобках, котельных, погребах первым делом необходимо обеспечить максимальное проветривание с кратностью газообмена 3-4 единицы в течение часа.
Основное применение
CO2 широко применяется в промышленности и в быту – в огнетушителях и для изготовления газировки, для охлаждения продуктов и для создания инертной среды при сварке.

Основное применение углекислого газа
Применение углекислого газа отмечено в таких отраслях, как:
для чистки поверхностей сухим льдом.
Фармацевтика
- для химического синтеза компонентов лекарственных средств;
- создания инертной атмосферы;
- нормализация индекса pH отходов производства.

Углекислый газ в фармацевтике
Пищевая отрасль
- производство газированных напитков;
- упаковка продуктов питания в инертной атмосфере для продления срока годности;
- декаффеинизация кофейных зерен;
- замораживание или охлаждение продуктов.

Углекислый газ в пищевой отрасли
Медицина, анализы и экология
- Создание защитной атмосферы при полостных операциях.
- Включение в дыхательные смеси в качестве стимулятора дыхания.
- В хроматографических анализах.
- Поддержание уровня pH в жидких отходах производства.

Углекислый газ и экология
Электроника
- Охлаждение электронных компонентов и устройств при тестировании на температурную стойкость.
- Абразивная очистка в микроэлектронике (в твердой фазе).
- Очищающее средство в производстве кремниевых кристаллов.
Химическая отрасль
Широко применяется в химическом синтезе в качестве реагента и в качестве регулятора температур в реакторе. CO2 отлично подходит для обеззараживания жидких отходов с низким индексом pH.

Использование углекислого газа
Применяется также для осушения полимерных веществ, растительных или животных фиброматериалов, в целлюлозном производстве для нормализации уровня pH как компонентов основного процесса, так и его отходов.
Металлургическая отрасль
В металлургии CO2 в основном служит делу экологии, защиты природы от вредных выбросов путем их нейтрализации:

Применение углекислого газа в металлургии
- В черной металлургии — для нейтрализации плавильных газов и для донного перемешивания расплава.
- В цветной металлургии при производстве свинца, меди, никеля и цинка — для нейтрализации газов при транспортировке ковша с расплавом или горячих слитков.
- В качестве восстановительного агента при организации оборота кислотных шахтных вод.
Сварка в углекислой среде

Процесс сварки с применением углекислого газа
Разновидность сварки под флюсом является сварка в углекислой среде. Операции сварочных работ с углекислым газом осуществляется плавящимся электродом и распространен в процессе монтажных работ, устранении дефектов и исправления деталей с тонкими стенками.
[править] Свойства
Получение углекислого газа Сухой лед — Удивительная подборка экспериментов с сухим льдом! (Химия) // Thoisoi Удушающий газ, без цвета и запаха, является естественной составляющей атмосферы Земли. Углекислый газ является продуктом сжигания ископаемого топлива. Он способствует удержанию тепла на поверхности Земли и вносит основной вклад в глобальное потепление.
При температуре 20 °C в 1 объеме воды растворяется 0,88 объемов CO2. Водный раствор его имеет кисловатый вкус. В отличие от монооксида, диоксид углерода является солеобразующим оксидом — ангидридом угольной кислоты H2CO3.
Под давлением около 60 атм диоксид углерода при обычной температуре превращается в жидкость. В сжиженном состоянии в стальных баллонах его можно хранить и транспортировать. При сильном охлаждении он превращается в снегообразную массу (сухой лед), которая сублимирует (испаряется, не плавясь) при −78,5 °С.
Диоксид углерода не поддерживает дыхание и горение обычных видов топлива. Но некоторые активные металлы могут отнимать у него кислород. Так, например, зажженная свеча гаснет в атмосфере CO2, а зажженная магниевая лента продолжает гореть:
2Mg + CO2 = 2MgO + C
Незначительные количества CO2 безвредны для человека и животных, но при концентрации его в воздухе более 3 % по объему он становится вредным, а при 10 % и более — смертельным.
Воздействие на человека
Углекислый газ нетоксичен, но при вдыхании его повышенных концентраций в воздухе по воздействию на воздуходышащие живые организмы его относят к удушающим газам. По ГОСТу (ГОСТ 8050-85) углекислота относится к IV классу опасности.
Незначительные повышения концентрации, вплоть до 0,2−0,4 % (2000−4000 ppm), в помещениях приводят к развитию у людей сонливости и слабости.
| Влияние на взрослых здоровых людей | Концентрация углекислого газа, ppm |
|---|---|
| Нормальный уровень на открытом воздухе | 350—450 |
| Приемлемые уровни | <600 |
| Жалобы на несвежий воздух | 600—1000 |
| Максимальный уровень стандартов ASHRAE и OSHA | 1000 |
| Общая вялость | 1000—2500 |
| Возможны нежелательные эффекты на здоровье | 1000—2500 |
| Максимально допустимая концентрация в течение 8 часового рабочего дня | 5000 |
Опасными для здоровья концентрациями считаются концентрации около 7−10%, при которых развиваются симптомы удушья, проявляющиеся в виде головной боли, головокружения, расстройстве слуха и в потере сознания (симптомы, сходные с симптомами высотной болезни), эти симптомы развиваются, в зависимости от концентрации, в течение времени от нескольких минут до одного часа.
Для помещений нормальным является уровень CO₂ около 600 ppm (частей на миллион). Повышенные концентрации углекислого газа снижают когнитивные способности людей. Уже при 1200 ppm расширяются кровеносные сосуды в мозге, снижается активность нейронов и уменьшается объём коммуникации между регионами мозга. В школьных классах типичной является концентрация 2000−2500, а общий разброс значений — от 1000 до 6000, это вызывает обеспокоенность у исследователей, поскольку выявлено снижение результатов учеников, выполняющих тестовые задания в душных помещениях.
При вдыхании воздуха с очень высокими концентрациями газа смерть наступает очень быстро от удушья, вызванного гипоксией.
Несмотря на то, что даже концентрация 5—7% CO₂ в воздухе несмертельна, но при концентрации 0,1 % (такое содержание углекислого газа иногда наблюдается в воздухе мегаполисов), люди начинают чувствовать слабость, сонливость. Это показывает, что даже при высоком уровне кислорода, большая концентрация CO₂ существенно влияет на самочувствие человека.
| Симптомы у взрослых здоровых людей | Концентрация углекислого газа, ppm |
|---|---|
| Легкое отравление, учащается пульс и частота дыхания, тошнота и рвота | 30 000 |
| Добавляется головная боль и легкое нарушение сознания | 50 000 |
| Потеря сознания, в дальнейшем — смерть | 100 000 |
Вдыхание воздуха с повышенной концентрацией этого газа не приводит к долговременным расстройствам здоровья. После удаления пострадавшего из атмосферы с высокой концентрацией углекислого газа быстро наступает полное восстановление здоровья и самочувствия.
При пониженном уровне углекислого газа в крови также возможен обморок. См. Гипервентиляция в статье “Лёгкие человека”.
Определение выбросов загрязняющих веществ
Для оценки экологической нагрузки, генерируемой котельной, важно уметь рассчитывать объем выбросов в атмосферу разных типов вредных соединений. Нормативы удельных выбросов для котельных установок. Нормативы удельных выбросов для котельных установок
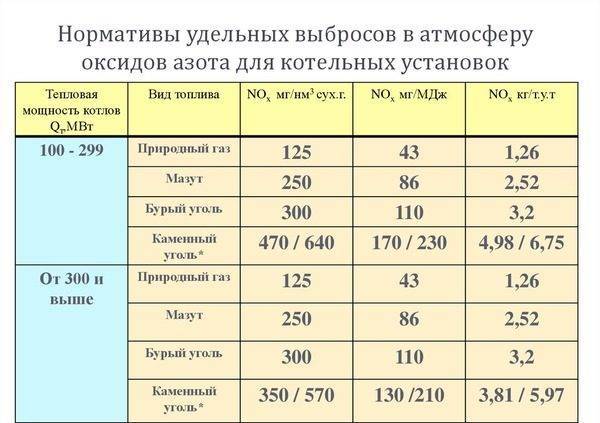 Нормативы удельных выбросов для котельных установок.
Нормативы удельных выбросов для котельных установок.
Газообразных
Рассчитать количество выбрасываемых в атмосферу окисей серы можно по такой формуле:
Mso2 = 20 * B * Sp (1-n’so2)(1-n»so2), в которой:
- В — расход использованного топлива, кг/с;
- Sp — процент серы в топливной массе;
- n»so2 — окиси в сыром золоуловителе;
- n’so2 — доля оксидов серы, связанных зольными соединениями внутри котлов.
Для окиси углерода формула будет иметь вид:
MCO = 10-3 * B * QpH *KCO (1-q4*0,01), в которой:
- В — расход топлива, г / с;
- QpH — наименьшая теплота сгорания;
- q4 — потери, связанные с неполным сгоранием;
- KCO — коэффициент образования окиси на единицу выделенного тепла, кг / Гдж (с неподвижной решеткой он будет равен 2 — для углей и 1 — для антрацитов).
Выбросы азотных оксидов при использовании твердого топлива в год вычисляют с помощью формулы:
MNO2 = Bp *QpH * KNO2 * βp* kп, и здесь:
- Bp — топливный расход;
- QpH — тепловая мощность котлов;
- KNO2 — удельный выход газа для сжигаемого топлива;
- βp — коэффициент, учитывающий влияние рециркуляции дыма на образование рассматриваемого газа (для твердотопливных систем он равен 1 — 0,075, где р — процент газовой рециркуляции);
- kп — коэффициент пересчета: при вычислении выбрасываемого газа в тоннах за год его берут равным 0,001.
 Выбросы азотных оксидов.
Выбросы азотных оксидов.
Твердых
При использовании угольного топлива происходит выброс в воздух твердых частиц. К ним относятся топливо, не подвергшееся сгоранию, и летучие зольные соединения. Объемы таких выбросов, проникающих в атмосферу с дымовыми газами, в граммах в секунду можно вычислить таким образом:
Mтв =10* B(аун *Ар+q4 *QpH/32,68)(1-n3) , где
- аун — доля проникающих в атмосферу с газами зольных соединений;
- Ар — процент зольности используемого топлива;
- q4 — коэффициент потерь, связанных с неполным сгоранием (считать для бурых разновидностей и донецкого угля с коэффициентом, равным 6);
- n3 — выбросы в твердой форме, попадающие в золоуловитель (значение находится в пределах 75-85%).
Зачем нужна инсуффляция при эндоскопии?
В норме все отделы толстого кишечника человека имеют небольшой диаметр (в среднем 4-6 см). Кроме того, слизистая оболочка желудочно-кишечного тракта имеет множество складок, ямочек и своеобразных углублений в виде карманов. Они нужны для увеличения «рабочей» поверхности и нормального процесса пищеварения – продвижения и расщепления пищевых масс, всасывания питательных веществ.
Инсуффляция предполагает нагнетание в просвет пищевода и желудка или толстой кишки углекислого газа, для этого к эндоскопическому оборудованию подключается специальный аппарат – инсуффлятор. Современные модели позволяют не только регулировать уровень подачи газа, но и контролируют входное и выходное давление, а также способны подогревать углекислый газ.
Основная цель проведения инсуффляции – облегчение прохождения эндоскопа. Постепенное нагнетание газа позволяет расширить просвет пищевода или кишечника, что дает возможность беспрепятственно провести инструмент в желудок или по отделам толстой кишки.
Сначала инсуффляцию проводили воздухом, при этом специалисты отмечали, что болезненные ощущения при проведении обследования были выраженными. Более того, после манипуляции пациенты продолжительное время отмечали значительный дискомфорт: вздутие, боли в животе, ощущение распирания. После внедрения в практику инсуффляции углекислым газом общая удовлетворенность процедурой возросла в несколько раз – это связано с тем, что в отличие от воздуха углекислый газ всасывается быстрее в несколько десятков раз. Следовательно, неприятные симптомы выражены менее ярко и беспокоят пациентов значительно реже.
Среди преимуществ инсуффляции углекислым газом можно отметить:
- сокращение сроков проведения исследования – за счет облегчения работы для врача-эндоскописта продолжительность процедуры значительно сокращается;
- хорошая визуализация и высокая информативность – поле зрения специалиста расширяется, следовательно, вероятность диагностических ошибок минимальна;
- уменьшение неприятных ощущений во время процедуры, особенно боли в животе;
- отсутствие болезненности или дискомфорта после манипуляции;
- уменьшение интенсивности послеоперационных симптомов (например, боль после удаления полипов толстой кишки).
Именно поэтому современный вариант колоноскопии и других эндоскопических исследований подразумевает проведение инсуффляции углекислым газом.
Искусственные источники углекислого газа
Углекислый газ попадает в атмосферу и в результате человеческой жизнедеятельности. Самыми активными источниками в наше время считаются:
- Индустриальные выбросы, происходящие в ходе сгорания топлива на электростанциях и в технологических установках
- Выхлопные газы двигателей внутреннего сгорания транспортных средств: автомобилей, поездов, самолетов и судов.
- Сельскохозяйственные отходы — гниение навоза в больших животноводческих комплексах
Кроме прямых выбросов, существует и косвенное воздействие человека на содержание CO2 в атмосфере. Это массовая вырубка лесов в тропической и субтропической зоне, прежде всего в бассейне Амазонки.
Искусственный источник углекислого газа
Несмотря на то, что в атмосфере Земли содержится менее процента диоксида углерода, он оказывает все возрастающее действие на климат и природные явления. Углекислый газ участвует в создании так называемого парникового эффекта путем поглощения теплового излучения планеты и удерживания этого тепла в атмосфере. Это ведет к постепенному, но весьма угрожающему повышению среднегодовой температуры планеты, таянию горных ледников и полярных ледяных шапок, росту уровня мирового океана, затоплению прибрежных регионов и ухудшению климата в далеких от моря странах.
https://youtube.com/watch?v=8IkNnmhQo-A
Знаменательно, что на фоне общего потепления на планете происходит значительное перераспределение воздушных масс и морских течений, и в отдельных регионах среднегодовая температура не повышается, а понижается. Это дает козыри в руки критикам теории глобального потепления, обвиняющим ее сторонников в подтасовке фактов и манипуляции общественным мнением в угоду определенным политическим центрам влияния и финансово-экономическим интересам
Человечество пытается взять под контроль содержание углекислого газа в воздухе, были подписаны Киотский и Парижский протоколы, накладывающие на национальные экономики определенные обязательства. Кроме того, многие ведущие автопроизводители автомобилей объявили о сворачивании к 2020-25 годам выпуска моделей с двигателями внутреннего сгорания и переходе на гибриды и электромобили. Однако некоторые ведущие экономики мира, такие, как Китай и США, не торопятся выполнять старые и брать на себя новые обязательства, мотивируя это угрозой уровню жизни в своих странах.
Применение
По ряду оценок, потребление СО2 на мировом рынке превышает 20 млн. метрических тонн в год. Столь высокий уровень потребления формируется под влиянием требований пищевой промышленности и нефтепромысловых предприятий, технологий газирования напитков и других промышленных нужд, например, снижения показателя Ph установок водоочистки, проблем металлургии (в том числе использования сварочного газа) и т.д.
Потребление углекислого газа неуклонно растет, поскольку расширяются сферы его применения, которые охватывают задачи от промышленного назначения до пищевого производства – консервация продуктов, в машиностроении от сварочного производства и приготовления защитных сварочных смесей до очистки поверхностей деталей гранулами «сухого льда», в сельском хозяйстве для подкормки растений, в газовой и нефтяной промышленности при пожаротушении.
Этиология и патогенез
Первая помощь должна быть оказана максимально оперативно, так как угарный газ быстро диффундирует через легочную капиллярную мембрану и связывается с железной частью гемма. Это происходит с примерно в 240 раз большей аффинностью, чем с кислородом.
Степень гемоглобинемии окиси углерода (CO-Hb) является функцией относительного количества СО и кислорода в воздухе, продолжительности воздействия и объема дыхания в минуту.
Некурящие могут иметь до 3% СО в крови, в то время как курильщики имеют уровни 10-15%.
Когда СО связывается с гемом, способность выделять кислород непосредственно в периферическую ткань организма снижается. Таким образом, дефицит кислорода происходит в тканях. CO влияет на периферическое потребление кислорода несколькими способами.
Концентрация СО в атмосфере обычно ниже 0,001%, но она выше в городских районах и в закрытых помещениях.
Большинство смертельных отравлений угарным газом происходит из-за пожаров, утечек в печах, портативных источников питания, работающих на бензине, гриля в помещении, выхлопных газов автомобилей. Угарный газ быстро всасывается в легкие. Выделение зависит от степени оксигенации и, в меньшей степени, минутного объема.
- Период полувыведения СО, когда человек дышит обычным воздухом, составляет около 300 минут.
- Если вы дышите богатым кислородом воздухом через маску, которая фильтрует выдыхаемый воздух, период полураспада составляет около 90 минут.
- При 100% гипербарическом кислороде это около 30 минут.
Вероятность смертельного исхода отравления возрастает при отсутствии своевременной помощи.